органична химия
Органичната химия. RANGE ВРЪЗКИ
За имената на органични съединения, използващи множество системи, но никой от тях не са подходящи за всички връзки. Консервирани много тривиални имена, които или са използвани още в началния етап на органичната химия и отразяват източник на качеството или характеристиките на, или са нови несистематични имената се използват заради удобството. Така че, CH3OH алкохол понякога се нарича "дърво на алкохол", тъй като е един път, изготвен от сухата дестилация на дървесина; системно име за този алкохол - метанол. Алкалоид морфин, наречен за своите наркотичен ефект, но в този случай общото име е единственият често се използва като системно име е трудно и тромаво. Тривиални имена често се дават на промишлени продукти, особено във фармацевтичната индустрия, където продуктите се продават под марката имена, едно и също съединение може да освободи различни фирми под различни имена. Често се използва kvazisistematicheskie имена, които не могат адекватно описват структурата на съединение, без допълнителна информация. Например, инсектицид ДДТ понякога се нарича dihlordifeniltrihloretanom, което не е достатъчно, за да напишете уникална структура на това съединение, тъй като името не казва нищо на позицията на хлорни атома. Пълното име за главните активни компоненти - 2,2-ди (4-хлорофенил) -1,1,1-трихлоретан.
Основните правилата на IUPAC наименования на съединенията съгласно системата са дадени по-долу: 1. Виж най-дългата непрекъсната верига от въглеродни атоми в молекулата. Името на съответния въглеводород се използва като основа за името на връзката. 2. атоми (различни от водород) и групи по веригата са дадени тук, и тези тук писмено преди името на основната въглеводород. 3. въглеродни атома основната въглеводородна верига са номерирани последователно, започвайки от края, така избран, че въглеродните атоми, носещи заместители, най-малък брой получени. 4. Регламент lokantami посочва заместителя - заместители номера преди посочващи серийни номера на въглеродните атоми към които те са свързани. 5. Ако има няколко идентични групи, се поставя преди името "ди" префикс "три", "тетра", "пента-" "хекса" и т.н. посочващ броя на групите присъстват. 6. двойни въглерод-въглеродни връзки На показват наставка "ен" ( "диен", ако две от тях и т.н.), и тройна - наставка "ин" ( "диен, установено" за две, и т.н.); при използване на тези наставки, завършващи "ен" се понижава. Предоставяне на множествени връзки означават серийни номера на въглеродни атоми, както се прави за заместителите. 7. Марк е изписано името дума. Няколко примера илюстрират тези правила:

Определяне такива сложни радикали като CH3CHCH2Cl в последния пример, се извършва съгласно следните правила: 1. въглероден атом с "свободен" връзката е номерирана 1. Най-дългата въглеродна верига, започвайки от тази точка, последователно номерирани и се използва за името на база (в този пример - етан). 2. хранени заместители, по веригата, както е описано по-горе в именуване на съединенията. 3. Пълно име на комплекс радикални затворени в скоби, за да се избегне объркване с цифрите за останалата част от молекулата. Имена IUPAC име конвенционална система за множество чести сложни радикали, дадени в таблица. 2. циклични въглеводороди наричат чрез добавяне на името на въглеводород с права верига с префикс "цикло". За отбелязване заместителят позицията на атомите в пръстена са номерирани последователно, като се започне с основните заместителите (таблица. 3).
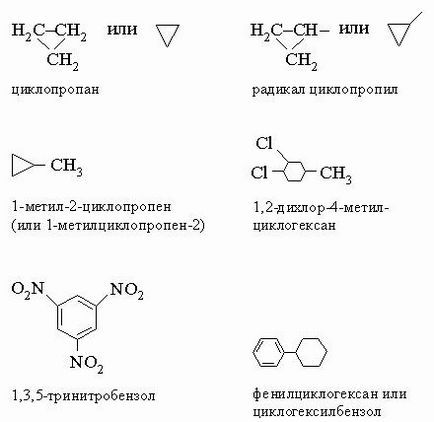
Забележете, че в този последен пример нарича просто въглеводород бензен (вместо 1,3,5-tsiklogeksatrienom) и съответния радикал - фенил.
По-сложните циклични съединения обикновено са дадени тривиални имена и системата за номериране. Съединения от този тип включват полициклични ароматни въглеводороди (бензенови пръстена, които са свързани с два общи атома) и хетероциклични съединения (която включва пръстенна структура хетеро). Ключови пръстенни системи и номериране са показани в таблица. 4. Забележете, че в хетероцикли номерация започва с хетероатоми и се прави така, че друг хетеро получи най-малък номер. Име заместители в тези пръстени следват основните правила на IUPAC-горе.
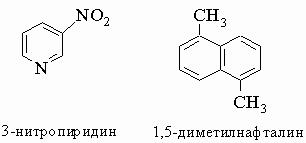
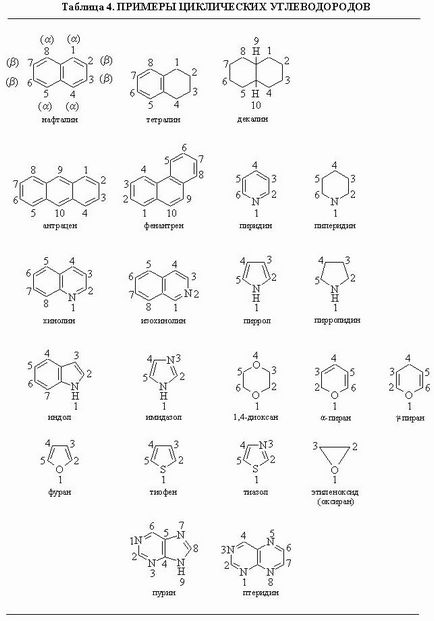
Таблица 4. ПРИМЕРИ ЗА цикличен въглеводород
Най-широко използвани за построяване на имената органични съединения IUPAC правила препоръчват използването на номенклатурата замяна. Общата схема на тези имена: 1) префикси - странична верига, след това долната функция (виж таблица 3) по азбучен ред .. 2) корена - основната верига или пръстен; 3) наставки - множество връзки, основната функция. например
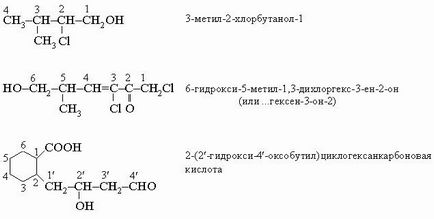
Геометрични изомери означени префикси цис- и транс- (см. По-горе). Оптичните изомери са означени чрез символа D-, L-, или мезо - преди името на връзката към зададени номера, към който принадлежи. Други системи се използват по-рядко. Посоката на въртене на равнината на поляризираната светлина често посочва знака (+) за дясновъртящ и (-) знак, за който лявовъртящият изомер. За киселини, но техните системни имена в научната литература са широко използвани тривиални имена. Някои важни органични киселини, изброени по-долу (Таблица. 5 и 6).
Производни на бензена, често имат общи имена, които са преобладаващи. Така че, апгинобензен нарича анилин и хидроксибензен - фенол. Дизаместени бензенов пръстен може да бъде наречена, nomeruya пръстенни въглеродни атома, както е обсъдено по-горе, или с помощта на префикс орто (о), мета (т) и пара (р) групи стоят заедно чрез един или два въглеродни незаместен, съответно. Например,
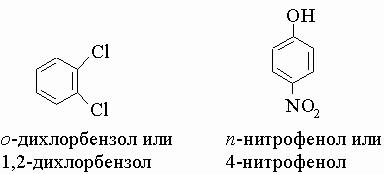
(Вж. Под "Реакциите на органичните съединения", Sec. IV-3 А)
Междинните частици. В много реакции са въвлечени междинни частици с изключително висока реактивност. черно карбаниона въглерод е отрицателно зареден; карбанйоните -Strengths база, те имат склонност да капан протон или ядрена атака положителни центрове. Както карбениевият йони (карбокатиони) Сажди е положително заредена; карбокатиони центрове са склонни да атакуват високо електронна плътност (атоми, олефинови връзки, ароматна система). Карбени са незаредени частици, имащи само шест електрони при въглерод; Те влизат в химични реакции, като се опитва да допълни секстет си на октет. Свободните радикали не се таксуват, но имат несподелена и свободен електрон и е също силно реактивни. Тези четири вида реактивни видове са представени по-долу протозойни техни представители метан производни: