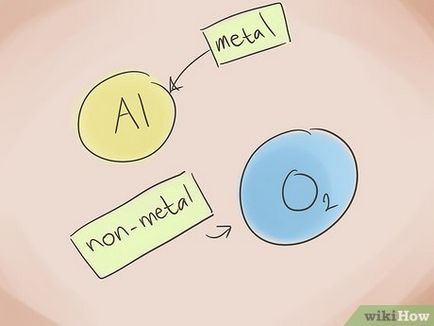
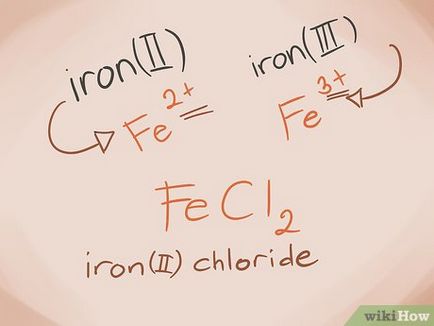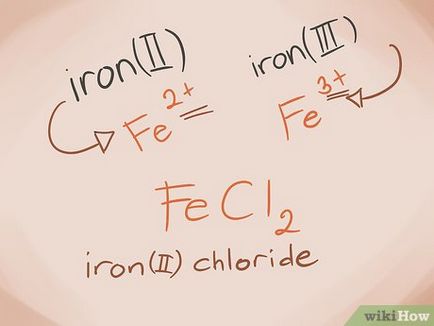Направете име. Наречен два елемент йонно съединение лесно. В първата част на името - на името на неметална елемент с наставката "-id". Във втората част на името - името на металния елемент в родителен падеж.
- ПРИМЕР: Al2 О3. Al2 = алуминий; О3 = кислород (кислород). Съответно, името на това съединение - "алуминий".
Научете се да се идентифицират метали с променлива валентност. Метали в блокове D и Е се наричат периодични система метали с променлива валентност. При формирането на наименованието на съединението на валентност написана като римски цифри. Това се дължи на факта, че те могат да имат повече от една валенция, и че те могат да образуват повече от едно съединение на друг атом.
- ПРИМЕР: FeCl2 и FeCl3. Fe = желязо; Cl2 = -2 хлорид; Хлорид CL3 = -3. Името ще бъде: железен хлорид (II) хлорид и желязо (III).
Метод 2 на 3:
Имена полихидритен съединения Редактиране
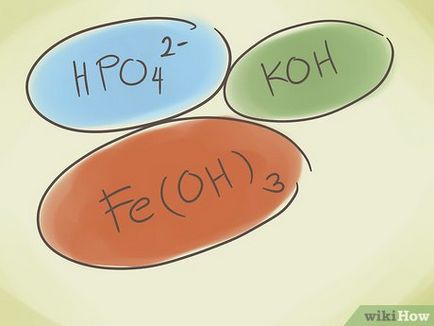
Разберете какво полихидрокси съединение. Тези съединения се състоят от групи от атоми, свързани един с друг, цялата група има положителен или отрицателен заряд. Можете да извършвате с многоатомни съединения са три основни операции:
- Добавянето на водороден атом в началото съединение. След това думата "хидро" се добавя в началото на името на съединение. Това намалява отрицателния заряд на устройството. Например, "карбонат" CO3 2- стане "водород" HCO3 -.
Почистете кислородния атом на съединението. Таксата ще останат същите, както и в края на смяната на съединение име от "-в" на "-um". Например: прехода от NO3 да NO2 - преход от "нитрат" с "нитрит".
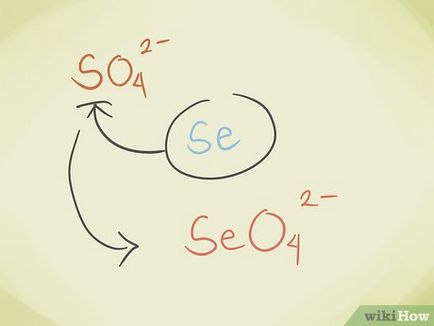
Замяна на централния атом на друга от същата група на периодичната система. Например, SO4 2- сулфат може да стане селенат SeO4 2-.
Не забравяйте общите комплексни йони. Тези йони - основа за образуване на по-голямата част от имената на многоатомни съединения. Те са изброени по-долу, за увеличаване на отрицателен заряд:
- Хидроксиден йон: ОН -
- Нитрат йон: NO3 -
- Бикарбонат йон: HCO3 -
- Перманганат йон: MnO4 -
- Карбонат йон: CO3 2-
- Хромат йон: CrO4 2-
- Бихромат йон: CR2 О7 2-
- Сулфат йон: SO4 2-
- Сулфит йон: SO3 2-
- Тиосулфат йон: S2O3 2-
- Фосфатен йон: PO4 3-
- амониев йон: NH4 +
Създаване на заглавните съединения на базата на този списък. Комбинирайте името на който и да е елемент или елементи, свързани с комплекс йон, и се обадете връзка. Ако елементът е изправена пред сложен йон, име на елемента е просто поставен след името на йон.
- ПРИМЕР: KMnO4. Виждаме, че MnO4 йон - - перманганат. К - е калий, така че името на съединението - калиев перманганат.
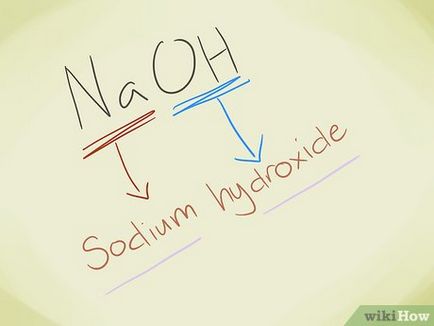
Пример: NaOH. Виждаме, че ОН - - е хидроксид йон. Na - натриев обаче титулните съединения - натриев хидроксид.