Амини - химическа енциклопедия
АМИНИ [от ч (MIAK)], NH3 производни. Н атоми в к-ryh заместени Org. остатъци R. В зависимост от броя на R е разделен на първични амини RNH2. RR'NH вторичен и третичен RR'R "N; R, R ', R" MB еднакви или различни. Sootv.-NH2 наречен. първичен амин, и -vtorichnoy-третичен. Според броя на аминогрупи в молекулата се разграничат моно-, ди-, три- и полиамини.
Имена амини, образувани от организационни имена. остатъци, свързани с атом N, напр. СН3 NH2 -метиламин, СН3 NHS3 H7 - метилпропиламин, (С2 Н5) 3 N - триетиламин. Също така се използва наименованието образува чрез добавяне на префикс "амино", "диамино" и т.н. за определянето на родовия въглеводород. например съединения от тип С2 Н5 СН (NH2) СН2 СН3 - 3-аминопентан. Много ароматни. Амини са тривиални имена, напр. С6 Н5 NH2 - анилин. СН3 С6 Н4 NH2 - Толуидини и OS6 Н4 СН3 NH2 - анизидин (съответно от "толуен" и от "анизол."). Висше alifatich. нормалната структура понякога се нарича амини. имена на мастни радикали с-т, единият от които се синтезират амини, напр. стеариламин. trilaurilamin.
спектри характеристика IR разтягане вибрации на NH връзки в р-D наблюдава за първични алкиламини в региони 3380-3400 см1 и 3320-3340 см -1; за първични ароматни съединения. амини - две абсорбционни ивици в региона 3500-3300 cm -1 (поради симетрични и асиметрични разтягане вибрации на М-Н връзки); за alifatich. и ароматни съединения. вторичен amiov-он лента съответно. в региона 3360-3310 см1 и 3500-3300 см1 регион; третични амини в тази област не се абсорбират. В NMR спектрите на химикал. амино протон смяна на 1-5 ррт Alifatich. амини в ултравиолетовата и видими региони не поглъщат ароматните. амини в UV спектъра имат две абсорбционни ивици, дължащи възли.
Алкиламини, силни основи. ариламини малко оси novny. При взаимодействието. минерално-трет амини за образуване на соли. в повечето случаи, р-в водоразтворим. RNH2 + НС1 -> [RN3] Cl -. Когато реакцията. напр. първични амини с алкилхалогениди амини води до получаване смеси от различни степени на алкилиране. и кватернерни амониеви соли.
При загряване. с въглерод-тер, техните анхидриди. хлоро-естери или анхидриди, първични и вторични амини ацилирани да образуват N-заместени амиди, напр. RNH2 + CH 3 COOH -> RNHCOCH3 + H2O анхидриди реагират при меки условия, още по-лесно - хлориди. к-ацилиране се провежда в присъствие на rymi. база. свързване, образуван в НС1 р-ТА. Когато поликондензация на диамини с дикарбоксилни до трето, са оформени техните естери или киселинни хлориди полиамиди. ВАцилираният амини имат слаби основни комуникационни-ти.
Под действието на HNO2 alifatich. първични амини се превръщат в алкохоли с разпределение N2 и Н2 О, вторични - N-нитрозамини в R2 nНяма да. Третични амини с обичайната т-RE с HNO2 не реагира. P-ТА с HNO2 използва за идентифициране alifatich. амини. При взаимодействието. първичен ароматен. HNO2 амин диазониева сол, образувана в кисела среда. ArNH2 + HNO2 + НС1 -> ArSl - + 2Н2 О. В същите условия, вторични ароматни. амини се превръщат в N-нитрозамини, третичен - ал-нитрозо производни. Основно alitsiklich. амини HNO2 форма алкохоли. че често е придружено от свиване или разширяване цикъл (вж. Demyanova пренареждане).
Alifatich. първични и вторични амини взаимодействие. с C12 или Br2. образуване на N-хало. Първични амини с фосген до получаване на изоцианат RNCO SOS12 или дизаместен карбамид (RNH) 2 CO, вторични амини - тетразаместен урея R2 NCONR2. Първични амини лесно взаимодействия. с алдехиди. като азометини (Шифови бази), например.
В реакцията на първични и вторични амини с етиленов хлорхидрин образува хидроксиетил производни като: С6 Н5 NH2 + S1SN2 СН2ОН -> С6 Н5 NHCH2 СН2ОН + HCI. В повечето случаи синтеза на същите тези комп. се използва етилен оксид. Lesko реагира с амини в присъствие. малък брой в Н 2О:
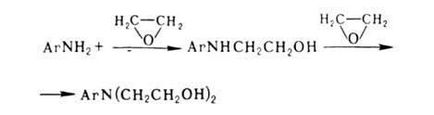
Тъй като скоростта на алкилиране на първия и втория етапи са същите, за получаване на моноалкил производно на етилен оксид се смесва в количество много по-малък изчислява.
Tsianetilnye производни на първични и вторични амини, получени р-ТА на акрилонитрил в присъствието. до-ви или основа. ArNH2 + = СН2 CHCN -> ArNHCH2 СН2 CN. Основното и средното alifatich. амини в взаимодействието. образуват соли с CS2 алкилови дитиокарбамати:
При загряване. първичен ароматен. амини с CS2 в присъствие. алкали образува diariltiomocheviny производни на-ryh -Важни ускорители на вулканизацията.
Хидрохлориди на третични амини по време на нагряването. с разредена. до трето dezalkiliruyutsya: (CH3) 3 HCl -> (CH3) 2 NH + CH3 С1.
Под влияние на силни окислители. напр. KMnO4. първичен alifatich. амини се превръщат в сместа в по рояк преобладават алдехиди. първичен ароматен. амини - до хинони и техни производни, вторичен alifatich. и ароматни съединения. амини - до четирикратно хидразин. При окисляването на третични амини действие на Н 2О 2 или перкиселини генерира N-оксиди на амини.
При заместването на ядрото в ароматния серия. амин амино ориентира електрофил. орто и пара-позиция, и по-силно кисела среда, поради протониране атом N - и в мета позиция. Нитрирането на ароматния първичен. амини усложнени от тяхното окисляване. обаче предварително ацилиран амин.
DOS. Ind. амин методи на синтез.
1. взаимодействие. алкохоли с NH3 (амонолиза алкохоли) в присъствието. дехидратация катализатори (напр. A12 О3. SiO2. ThO2. алуминосиликати. метални фосфати) при 300-500 ° С и 1-20 МРа. Това произвежда смес от първични, вторични и третични амини. ROH + NH3 -> RNH2 R2 NH RAN; едновременни диспропорциониране амини. 2RNH2 -> R2 NH + + NH3. R2 NH + RNH2 -> R3 N + NH3. 2R2 NH -> R3 N + RNH2. Този метод се използва за производствени острови alifatich по-ниска. амини. и особено метил и ethylamines. Синтез придружава от образуване средства. Номер в страничните продукти - олефини.
Ако се получат NH3 вместо използване на първични или вторични амини и вторични (или третични амини). Този метод (аминолиза) циркулира за производство острови N-алкил- и N, N-dialkylanilines. Той разработи подобен метод за получаване на анилин взаимодействие. фенол с NH3. Лесно е да се реагира с NH3 Аминонафтоли. образуващи нафтиламини (вж. Bucherer реакция).
2. Възстановяване. аминиране alifatich. и tsikloalifatich. в присъствието на алкохоли. Н2 на катализаторите на дехидрогениране хидрогениране-(N1, Co, Cu-повишен Fe). Процесът се провежда при 150-250 ° С и 0.1-5 МРа:
Алкохоли могат да бъдат използвани вместо алдехиди или кетони; при което се образува смес от първични и вторични амини.
3. Katalitich. хидрогениране на нитрили (kat.-Ni или Co) при 100-130 ° С и 0.1-10 МРа. С добри добиви първични амини до вторична смес:
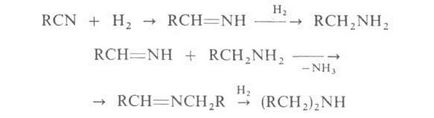
Този метод се използва Chap. Пр. за производство на островите по-висока първична и вторична alifatich. нормалната структура на амини.
5. P-ционни alifatich амиди. и ароматни съединения. карбоксилна-т-р алкален рами С12. I2 или Br2 да образуват първични амини. В този случай въглеродната верига е съкратен с един атом (Hofmann реакция).
6. P-TION с алкилови и арилови халиди. Чрез кондензация на фталимид с алкилхалогениди на последния. хидролиза (вж. Gabriel реакция) са чисти първични алифатни амини.
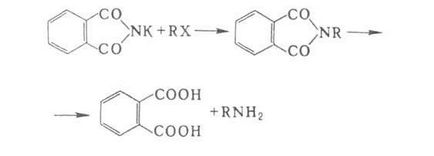
Арил халогениди реагират с NH3 и амини трудно, така че в бала-STI използват Conn. за халоген-активиран ryh силни електрон-отнемане заместители, по-често, нитро или сулфо. По този начин декември дифениламин и производни на нитроанилини.
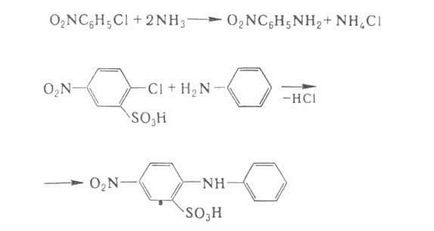
Амонолиза и аминолиза на арилови халиди с неактивирани халоген изисква прилагане Ser. Cu като катализатор.
7. нитрозиране N, N-dialkylanilines на плацентата. хидролиза (подготовка alifatich чист вторичен амин.):
В лабораторни синтезира амини, напр. р-ции Уолах Delepine, наCurtus за, Leuckart, загуба, Манихови.
Специфика. р-ТА откриване амини. първични амини с нагряване. с СНС13 в присъствие. алкален трансформира в изонитрили. като много остра миризма: RNH2 + СНС13 -> RNC + ZNS1; вторични амини в обработката на HNO2. последък. сливане на получената утайка с фенол и подкисляване с конц. H2 SO4 се появява зелен цвят. За идентифициране на първични и вторични амини се използват в ацилиране на амиди. За количества. определяне на амини, използвани Kjeldahl методи и Van SLYKE (за първична alifatich. амини) bromometrich. метод, титруване р-до-посочени във водни и неводни носители, газово-течна хроматография. Основно ароматен. амини също определят фотометрично след образуване на съответните Шифови бази или азосъединения.
Alifatich. амини засягат нервната система причинява смущения пропускливост на стените на кръвоносните съдове и клетъчни мембрани. F-ции на черния дроб дистрофия и развитие. Ароматен. амини предизвика образуването на метемоглобин. инхибиторен център. нервната система. Nek- ароматен. А канцерогени, което води до рак на пикочния мехур в човека (напр. Р-нафтиламин, бензидин. 4-аминобифенил).
===
App. Литература за статията, "Амин". Тернов Modern Organic Chemistry. на. от английски език. т 2, Москва 1981. Общо органичната химия. на. от английски език. Vol. 3, М. 1982, стр. 11-91, 168-228; Ullmanns Encyklopadie, 4 Aufl. Bd 7, Weinheim, 1974: Кърк-Отмър енциклопедия, 3 изд. с. 2, N.Y .- [a.o.], 1978, стр. 272-376. BV Salol.